Wasserwerte
Der pH-Wert gilt in der Aquaristik als der
wichtigste „Wasserwert“, der ein Maß für den Säuregehalt des Wassers
darstellt. Lebewesen haben einen
unterschiedlich großen Toleranzbereich für den pH-Wert und können
außerhalb
von diesem nicht überleben. Die Überprüfung, ob eine Tierart in
einem
Aquarium geeignete Überlebensbedingungen findet, orientiert sich in
aller
Regel zuerst am pH-Wert. Der Toleranzbereich von Pflanzen ist meist
etwas
größer als der von Tieren.
Der pH-Wert wird auf einer logarithmischen Skala mit Werten zwischen
1 und
14 gemessen. Wasserwerte im Aquarium liegen zwischen 4,5 und 9,5,
wobei
beides Extremwerte darstellt. Ein pH-Wert von sieben gilt als
„neutral“,
d.h. weder als alkalisch noch als sauer. Logarithmisch bedeutet
dabei, dass
Wasser mit einem pH-Wert von sechs bereits 10 mal mehr Säuren als
solches
mit einem pH-Wert von 7 enthält. Wasser mit einem pH-Wert gar von
fünf
enthält bereits 100 mal mehr Säuren als solches mit einem Wert von
7. So
genannte Schwarzwasseraquarien, in denen südamerikanische Fische wie
etwa
Skalare oder der häufig gehaltene Rote Neon gut gedeihen, haben
beispielsweise pH-Werte im Bereich von 5,5 bis 6,5.
# pH < 7 entspricht einer Lösung mit saurer
Wirkung
# pH = 7 entspricht einer neutralen Lösung.
# pH > 7 entspricht einer alkalischen Lösung (basische Wirkung)
Wasserpflanzen gedeihen am besten in Aquarien mit einem pH-Wert
unter 7,
da bei diesen Werten in aller Regel auch der für das
Pflanzenwachstum
wichtige Kohlensäurewert höher ist. In Wasser mit einem pH-Wert über
7, das
als „alkalisch“ bezeichnet wird, fühlen sich vor allem
ostafrikanische
Barsche wohl.

Der Skalar benötigt für sein Wohlbefinden einen pH-Wert zwischen 5,5
und 6,5
Die Carbonathärte (KH) bezeichnet die Menge an
Carbonat- und
Hydrogencarbonat-Ionen. Damit diese Anionen als Carbonathärtebildner
fungieren können, muss eine entsprechende Anzahl von Calcium- und
Magnesium-Kationen vorhanden sein. Die Carbonathärte stellt im
Wasser einen Säurepuffer dar, der eine starke und schnelle
Veränderung des pH-Wertes
verhindert. Wasser mit einem niedrigen KH-Wert hat im allgemeinen
einen
niedrigen pH-Wert, während Wasser mit einem hohen KH-Wert
normalerweise
alkalisch ist.
Die Gesamthärte (GH) bezeichnet die Summe aller im
Wasser gelösten Ionen der Erdalkalimetalle. Zu diesen zählen neben
Magnesium und Calcium (ca. 80%) unter anderem Strontium und Barium.
In der Aquaristik spielt die Gesamthärte meist eine geringere Rolle
als die Carbonathärte. Normalerweise
ist die Karbonathärte geringer als die Gesamthärte.
# Weiches Wasser
ist günstiger für alle Anwendungen, bei denen das Wasser erhitzt
wird, zum Waschen, zum Gießen von Zimmerpflanzen etc. Weiches Wasser
steht in Regionen mit Granit, Gneis, Basalt und Schiefer-Gesteinen
zur Verfügung. Auch Regenwasser ist weiches Wasser.
# Hartes Wasser
führt zur Verkalkung von Haushaltsgeräten, erhöht den Verbrauch von
Spül- und Waschmitteln, beeinträchtigt den Geschmack und das
Aussehen empfindlicher Speisen und Getränke (z.B. Tee). Hartes
Wasser kommt aus Regionen, in denen Sand- und Kalkgesteine
vorherrschen
Mit dem Leitwert wird die Summe aller gelösten Salze im Wasser
bezeichnet. Je mehr Salze im Wasser gelöst sind, desto besser ist die
Leitfähigkeit. Vollentsalztes Wasser leitet kaum noch Strom (eine geringe
Leitfähigkeit ist durch die Eigendissoziation immer gegeben).
Der Leitwert spielt insbesondere dann eine Rolle, wenn Weichwasserfische
gezüchtet werden sollen.
Salzgehalt und Redoxpotential.
Eine Bestimmung des Salzgehaltes und des Redoxpotentials wird nur für Brackwasser- und Meereswasseraquarien benötigt.
Die Dichte des Salzgehaltes wird mit einem Aräometer gemessen. Süßwasser
hat bei einer Temperatur von 4 Grad Celsius ein spezifisches Gewicht von 1,0.
Tropisches Meereswasser, also das Meerwasser, das normalerweise in einem
Meerwasseraquarium nachgebildet wird, hat dagegen bei dieser Temperatur wegen
der gelösten Salze und Spurenelemente ein spezifisches Gewicht zwischen 1,020
und 1,027. Brackwasser liegt zwischen diesen beiden Werten. Die in der
Aquaristik verwendeten Aräometer sind auf 24 Grad Celsius geeicht.
Das Redoxpotential (rH-Wert) sagt aus, wie hoch das Wasser mit organischen Substanzen belastet ist und welchen Gehalt an Sauerstoff es aufweist. Hohe Werte deuten auf einen hohen Sauerstoffgehalt und einen geringen Gehalt an organischen Stoffen hin. Gemessen wird der rH-Wert mit elektronischen Messgeräten. Bei der Ermittlung der Werte müssen auch der pH-Wert sowie die Wassertemperatur berücksichtigt werden.
Stickstoffumwandlung im Aquarium
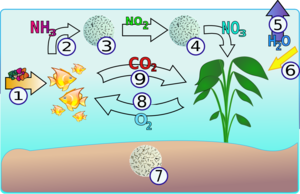
Stickstoffkreislauf im Aquarium
Die Stickstoffumwandlung, die durch Pflanzen und Mikroorganismen (einschl.
Filter) im Aquarium stattfindet, wird gelegentlich auch als Stickstoffkreislauf
bezeichnet. Bei den wenigsten Aquarien liegt jedoch tatsächlich ein Kreislauf
vor, bei dem keine Eingriffe mehr notwendig sind. Die Lebewesen im Aquarium sind
in der Regel auf Futter angewiesen und zur Nitratreduzierung ist ein
regelmäßiger Teilwasserwechsel notwendig. Über die Kiemen und aus dem Urin der
im Aquarium gepflegten Lebewesen sowie dem unverbrauchtem Futter wird zunächst
das giftige Ammoniak freigesetzt. In nicht zu alkalischem Wasser liegt diese
Stickstoffverbindung überwiegend als Ammonium vor. Dieses ist für die Fische und
Wirbellosen des Aquariums weniger schädlich. Für Pflanzen stellt es sogar einen
wertvollen Dünger dar. Lediglich bei hohen pH-Werten und Temperaturen überwiegt
Ammoniak. Für Fische stellt Ammoniak ein starkes Gift dar. Ist Ammoniak im
Wasser hoch konzentriert, sind diese nicht mehr in der Lage, über die Kiemen
Ammoniak abzuatmen. Sie vergiften sich dann letztlich selbst. Das Ammonium, das
von den Pflanzen nicht als Nährstoff verbraucht wird, wird von Mikroorganismen
wie z. B. Nitrosomonas-Bakterien, die sowohl im Aquarium als auch im Filter
vorhanden sind, in Nitrit abgebaut. Nitrit ist wie Ammoniak für Fische giftig
und bereits ab Werten von 1 Milligramm pro Liter tödlich. Ein plötzliches Hin-
und Herschießen der Fische im Aquarium, apathisches Verhalten oder hektisches
Atmen weisen auf eine mögliche Vergiftung durch Nitrit hin. Nitrit wird
allerdings durch z. B. Nitrobakter-Bakterien in der nächsten Stufe zu Nitrat
umgewandelt. Dieser Prozess, bei dem unter Verbrauch von Sauerstoff Ammonium zu
Nitrit zu Nitrat umgewandelt wird, wird als Nitrifikation bezeichnet. Nitrat ist
für Fische nicht giftig. Er sollte jedoch gering gehalten werden, um eine
(teilweise) Denitrifikation (s. u.) im Aquarium oder Körper des Fisches zu
vermeiden, die letztlich wieder Nitrit freisetzen würde. Nitrat wird daher durch
den regelmäßigen Teilwasserwechsel aus dem Aquarienwasser entfernt. Neben der
Nitrifikation findet noch ein weiter Prozess statt, bei dem von
Mikroorganismen Nitrat als Ersatz für Sauerstoff veratmet wird. Diesen anaerob
ablaufenden Prozess bezeichnet man als Denitrifikation. Er findet in den meisten
Aquarien kaum statt und kann bei Bedarf z. B. durch spezielle Filter unterstützt
werden.
# Anaerobie (v.
lat. aer „Luft“) bezeichnet Reaktionsbedingungen, die in Abwesenheit
von Sauerstoff ablaufen. Lebewesen, die für ihren Stoffwechsel nicht auf
Sauerstoff angewiesen sind, werden entsprechend als Anaerobier
bezeichnet. Anaerobe Prozesse sind von großer Bedeutung für den
Naturhaushalt. Der Begriff ist unter anderem bei der Kultivierung von
Mikroorganismen von Bedeutung. Die Empfindlichkeit der Mikroorganismen
gegenüber Sauerstoff macht es nötig, diese unter sauerstofffreien
Bedingungen zu kultivieren. Hierbei wird die so genannte Anaerobentechnik
verwendet.
Quelle:
Wikipedia:http://de.wikipedia.org/wiki/Aquarium#Chemie_im_Aquarium
Aktualisiert am:
23.08.20 19:16:24